di P. Wostyn, D. Van Dam, K. Audenaert, V. De Groot, in Fluids and Barriers of the CNS (2015)
Link all’articolo originale: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4485867/
Scarica l’articolo in formato .pdf
Le nuove scoperte di biologia molecolare indicano che la fisiologia del liquido cerebrospinale è molto più complessa di quanto si fosse ritenuto fino ad oggi. Recentemente la teoria classica sulla circolazione del liquido cerebrospinale (dai plessi corioidei ai ventricoli, cisterne e spazio subaracnoideo per essere assorbito all’interno del sistema venoso mediante i villi aracnoidei e/o attraverso gli spazi perineurali dei nervi cranici sino al sistema linfatico cervicale) è stata messa in discussione da una nuova ipotesi sull’idrodinamica del liquor [1,2].
Secondo questa nuova ipotesi il liquor viene costantemente prodotto e assorbito all’interno del sistema come conseguenza della filtrazione e del riassorbimento del volume dell’acqua attraverso le pareti dei capillari nel fluido interstiziale del tessuto cerebrale circostante [1-3]. Inoltre recenti scoperte hanno rivelato l’esistenza di una rete cerebrale di canali paravascolari chiamata via glinfatica. Su questa via, attraverso il parenchima cerebrale, ricircola una grossa quantità di fluido cerebrospinale subaracnoideo che facilita la clearance dei soluti interstiziali all’interno del cervello, incluso il peptide beta-amiloide [1,4) con le possibile implicazioni negli stadi preclinici della malattia di Alzheimer [5] e di altre malattie neurodegenerative.
Nel presente articolo vengono passati in rassegna alcuni studi che si basano sull’utilizzo della risonanza magnetica (RM) e forniscono un’opportunità unica per studiare il ruolo del sistema glinfatico nel glaucoma. Se tale ipotesi dovesse essere confermata porterebbe a una nuova comprensione della patogenesi del glaucoma.
Discussione
Il glaucoma è una malattia neurodegenerativa complessa
Il glaucoma è una delle maggiori cause di cecità in tutto il mondo [7].
La tipologia più comune è il glaucoma primario ad angolo aperto (GPAA) che è una malattia neurodegenerativa complessa caratterizzata da una lenta e progressiva degenerazione delle cellule gangliari della retina e dei loro assoni nel nervo ottico con conseguenti difetti del campo visivo [7].
La radice del nervo ottico è il probabile sito della lesione iniziale e l’aumento della pressione intraoculare è considerato come il maggior fattore di rischio per lo sviluppo del GPAA [7,8]. Tuttavia una pressione intraoculare elevata non è presente in tutte le forme del GPAA [7]. Infatti nel glaucoma a pressione normale la pressione intraoculare non è elevata, pertanto nella neuropatia ottica del GPAA dovrebbero essere coinvolti altri fattori di rischio [7].
Un numero crescente di prove supporta l’ipotesi che il liquido cerebrospinale (sia per la sua pressione che per la composizione) che circonda il nervo ottico possa avere un’importanza fondamentale nella patogenesi del glaucoma [9-12]. Il nervo ottico, tratto di materia bianca del sistema nervoso centrale (SNC), è incorporato in tutte e tre gli strati meningei e circondato da liquor nello spazio subaracnoideo con una pressione equivalente alla pressione intracranica [10,13]. Pertanto oltre alla pressione intraoculare il nervo ottico è esposto anche alla pressione intracranica [10]. La lamina cribrosa, la regione perforata della sclera attraverso la quale passano le fibre ottiche del nervo ottico, separa queste due zone pressurizzate [10].
L’accumulo di beta-amiloide può essere coinvolto nella morte delle cellule gangliari nel glaucoma
Ci sono sempre maggiori prove che indicano il beta-amiloide come fattore coinvolto nello sviluppo dell’apoptosi delle cellule gangliari nel glaucoma [14-17], suggerendo quindi un possibile legame con la malattia di Alzheimer. Precedenti studi hanno dimostrato che nel glaucoma l’aumento di beta-amiloide è correlato alla pressione intraoculare [14-17]. McKinnon et al. [14] hanno segnalato che nei ratti le cellule gangliari della retina, sottoposte a un aumento cronico della pressione intraoculare, mostrano un’elaborazione anormale di una proteina precorritrice della beta-amiloide (APP). Guo et al. [16] hanno dimostrato in vivo che il beta-amiloide causa una significativa apoptosi di queste cellule . Inoltre i ricercatori hanno provato un’efficace strategia di trattamento del glaucoma bloccando gli effetti della beta-amiloide tramite la terapia farmacologica [16].
Recentemente, in uno studio che ha utilizzato scimmie per il glaucoma sperimentale, Ito et al. [17] hanno riscontrato espressioni e localizzazioni tempo-dipendenti del beta-amiloide nella retina come anche nella radice del nervo ottico in seguito all’aumento cronico della pressione intraoculare.
Diminuzione dei livelli di beta-amiloide e aumento di quelli di tau nell’umore vitreo e nel liquido cerebrospinale
Gli studi riportano una diminuzione di beta-amiloide [1-42] e un aumento di quelli di tau nel liquido cerebrospinale in pazienti affetti da Alzheimer rispetto ai soggetti sani [20,21] dovute a un aumento dell’aggregazione, alla formazione di placca e fibrille e alla scarsa clearance di questi peptidi dal sistema nervoso centrale [22]. Per testare l’idea che il beta-amiloide [1-42] e il tau contribuiscano allo sviluppo del glaucoma, Yoneda et al. [21] hanno misurato le concentrazioni di queste due sostanze nei campioni di umore vitreo prelevati dagli occhi di pazienti affetti da glaucoma.
I ricercatori hanno riscontrato una diminuzione significativa dei livelli di beta-amiloide [1-42] nel vitreo (in linea con le sedimentazioni di beta-amiloide nella retina) e un notevole aumento dei livelli di tau nel vitreo di pazienti con glaucoma rispetto al gruppo di controllo [16,21]. Le loro scoperte suggeriscono che i processi neurodegenerativi nel glaucoma potrebbero condividere, almeno in parte, un meccanismo comune con l’Alzheimer [21].
Flusso dei fluidi nella parte anteriore del nervo ottico
È interessante notare che precedenti studi volti a investigare il flusso dei fluidi nella parte anteriore del nervo ottico, sembrano confermare la presenza di uno scambio di qualche tipo tra il fluido interstiziale del nervo ottico e il liquido cerebrospinale circostante. Tali studi hanno anche dimostrato che i fluidi del corpo vitreo e del nervo ottico si muovono da direzioni opposte e convergono alla radice del nervo ottico [24,25] che è riconosciuta come probabile sito della lesione iniziale [8].
Le probabili fonti del fluido interstiziale nella parte anteriore del nervo ottico sono i capillari del nervo stesso, la coroide peripapillare, il corpo vitreo, il liquido cerebrospinale e forse l’assoplasma negli assoni locali [24]. Alcuni studi hanno riscontrato la presenza di un deflusso del fluido dal corpo vitreo verso la testa del nervo ottico [24-26].
Rodriguez-Peralta [25] ha studiato la materia iniettando il colorante diamino-acridina nel corpo vitreo di un gruppo di animali dimostrando il movimento immediato della sostanza in direzione periferica verso la retina e verso la testa del nervo ottico [25], anteriormente rispetto alla lamina cribrosa. Quest’ultima è l’area in cui è stato possibile individuare la maggior concentrazione di diamino-acridina. Hayreh [24] ha studiato il deflusso dal corpo vitreo verso il nervo ottico nei macachi rhesus iniettando la leucina triziata nel corpo vitreo.
Le cellule gangliari e la parte interna della retina sono state precedentemente necrotizzate, di conseguenza non era presente alcun trasporto assoplasmatico [24], tuttavia la sostanza tracciante riscontrata nella testa del nervo ottico rappresentava un flusso diretto dal corpo vitreo al nervo, senza trasporto assoplasmatico [24]. Tali studi hanno rivelato un pesante accumulo di tracciante nelle cellule gliali della parte anteriore della regione prelaminare, un accumulo minore nella porzione posteriore della stessa regione, uno ancora minore nella lamina cribrosa e quasi nessuno nel nervo ottico retrolaminare [24]. In aggiunta a questo deflusso del fluido dal corpo vitreo verso la testa del nervo ottico, alcuni studi hanno stabilito l’esistenza di un flusso di fluido dallo spazio subaracnoideo del nervo ottico verso il nervo ottico e la testa del nervo [24,25,27,28].
Una via glinfatica per lo scambio di liquido cerebrospinale e fluido interstiziale nel nervo ottico?
Considerate nel loro insieme, le scoperte fino ad ora riportate suggeriscono quantomeno qualche tipo di scambio tra il fluido interstiziale del nervo ottico e il liquor circostante. Se viene paragonato alle dimensioni del cervello il nervo ottico è una struttura relativamente piccola, in tali piccole strutture anche la semplice diffusione di grandi soluti può risultare sufficientemente rapida per permettere la clearance (Iliff JJ, comunicazione personale, 2013). In ogni caso, oltre alla semplice diffusione o al deflusso convenzionale del liquido cerebrospinale, la domanda che si presenta è se il nervo ottico utilizzi o meno anche vie paravascolari per facilitare uno scambio più rapido. In quanto estensione del cervello (Figura 1), gli occhi riflettono tante similitudini con esso in termini di anatomia e funzionalità [13].
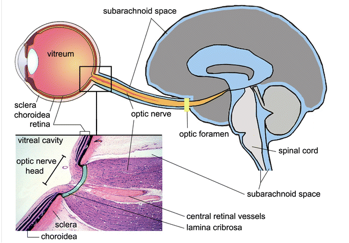
Sarebbe dunque interessante indagare se tale via glinfatica per lo scambio tra il liquido cerebrospinale e il fluido interstiziale esista nel nervo ottico. In ogni modo, anche se così non fosse potrebbe esserci una interconnessione tra la via glinfatica del cervello e lo spazio subaracnoideo del nervo ottico che potrebbe facilitare uno scambio efficace tra liquor e fluido interstiziale nel nervo ottico, permettendo così la clearance dei soluti interstiziali, incluso il beta-amiloide.
Esplorare questa possibilità potrebbe gettare nuova luce sulla patogenesi del glaucoma. Infatti se questa ipotesi venisse confermata ci si potrebbe aspettare che un sistema glinfatico disfunzionale del cervello possa in ultimo risultare in una scarsa clearance delle neurotossine nel nervo ottico e portare alla neurodegenerazione glaucomatosa. L’osservazione di un sistema glinfatico disfunzionale in pazienti affetti da glaucoma fornirebbe inoltre sostegno all’ipotesi che la disfunzione circolatoria del liquido cerebrospinale possa giocare un ruolo nella patogenesi del danno glaucomatoso.
L’ipotesi è che il glaucoma, come la malattia di Alzheimer, possa verificarsi quando è presente uno squilibrio tra produzione e clearance delle neurotossine, incluso il beta-amiloide [30]. Quindi, l’alterazione dominante determina se il glaucoma si manifesterà come glaucoma a tensione normale oppure a tensione alta. Nella tipologia a tensione normale, la clearance anormale di beta-amiloide nel nervo ottico può prevalere come risultato della disfunzione della via glinfatica.
Nel glaucoma a tensione alta invece può prevalere la generazione di beta-amiloide indotta dalla pressione intraoculare e anche un lieve problema nella funzionalità della via glinfatica può portare al danno glaucomatoso del nervo ottico.
Un numero crescente di prove indica che la pressione intracranica è minore in pazienti affetti da GPAA se paragonati al gruppo di controllo di soggetti non glaucomatosi, inoltre risulta minore nel glaucoma a tensione normale rispetto alla forma a tensione alta del GPAA [9-11].
Una pressione intracranica inferiore può essere la conseguenza della diminuzione nella produzione del liquido cerebrospinale oppure una ridotta resistenza al deflusso del liquor. In questo contesto è importante notare che un recente studio ha riscontrato che la pressione intracranica diminuisce notevolmente e costantemente dopo i 50 anni [31], dato che corrisponde all’aumento dell’incidenza del glaucoma con l’avanzare dell’età [31]. Non ci sono prove che la resistenza al deflusso del liquido cerebrospinale diminuisca con l’età, al contrario la maggioranza degli studi riporta un aumento della resistenza al deflusso del liquor [31,32], tuttavia ci sono prove della diminuzione della produzione di liquido cerebrospinale con l’età [31,33]. Pertanto una minore pressione intracranica individuata in pazienti affetti da GPAA potrebbe essere un indicatore della diminuzione della produzione e del ricambio di liquido cerebrospinale [7].
Il punto di vista qui esposto rende possibile la spiegazione della sovrapposizione clinica tra malattia di Alzheimer e glaucoma. Questa maggiore incidenza del glaucoma in pazienti affetti dalla malattia di Alzheimer in combinazione con le numerose similitudini tra queste due malattie ha sollevato la questione sul fatto che l’Alzheimer e il glaucoma potessero condividere un meccanismo di base comune [36]. Come potenziale meccanismo di collegamento la disfunzione della via glinfatica è un’ipotesi allettante poiché potrebbe spiegare le coincidenze tra questi due disturbi.
Ovviamente sono necessari ulteriori studi per far luce sul potenziale ruolo svolto dal sistema glinfatico nel glaucoma.
Conclusione
Il sistema glinfatico è stato recentemente definito come via cerebrale paravascolare per lo scambio tra liquido cerebrospinale e fluido interstiziale in grado di facilitare un’efficace clearance dei soluti interstiziali dal cervello, incluso il beta-amiloide. Una nuova teoria ipotizza che il fallimento di questo sistema di clearance sia alla base dell’accumulo di beta-amiloide nella malattia di Alzheimer. In questo articolo abbiamo raccolto alcuni studi che suggeriscono una potenziale rilevanza clinica del sistema glinfatico per la comprensione del glaucoma. È necessario sottolineare che almeno per il momento l’ipotesi qui esposta rimane non provata. Sono necessari ulteriori studi per determinare se il sistema glinfatico possa svolgere un ruolo patogenico nello sviluppo del glaucoma. Recentemente è stato accettato, a livello clinico, l’approccio della risonanza magnetica per valutare la funzione della via glinfatica negli esseri umani. Questa è un’opportunità unica per determinare se la soppressione del sistema glinfatico e, di conseguenza, la disfunzione circolatoria del liquido cerebrospinale contribuiscano allo sviluppo del glaucoma.